毛宗万、谭彩萍教授团队:钌配合物用于DNA相分离诱导与示踪发表于《Journal of American Chemical Society》
相分离过程异常与多种重大疾病的发生和发展相关联,如神经退行性疾病、发表于癌症和衰老等。对相分离过程的调控与示踪将有助于人们更好地理解这些疾病的发生机制,同时也可为它们的治疗提供新的策略。癌症的特征与控制基因表达谱的染色质状态变化密切相关,真核细胞通过液-液相分离(liquid-liquid phase separation, LLPS)在空间和时间上组织细胞质和核质,从而调节染色质可及性来协调基因的表达。能够在活细胞中诱导DNA LLPS的小分子还未见报道,研究的难点包括缺乏理性设计DNA LLPS诱导剂的构效关系、小分子有限的细胞核穿透能力以及活细胞内DNA LLPS的原位监测方法的缺失。
近日,永利集团3044noc登录入口毛宗万教授、谭彩萍教授团队与中国科学院大连化学物理研究所李国辉研究员、张跃斌副研究员团队合作,报道了第一例能够在活细胞中诱导DNA LLPS的小分子。DNA光开关Ru1能以高亲和力与DNA结合(图1),分子动力学模拟证明电荷相互作用和π-π堆积对其诱导DNA相分离的能力都起着重要作用。
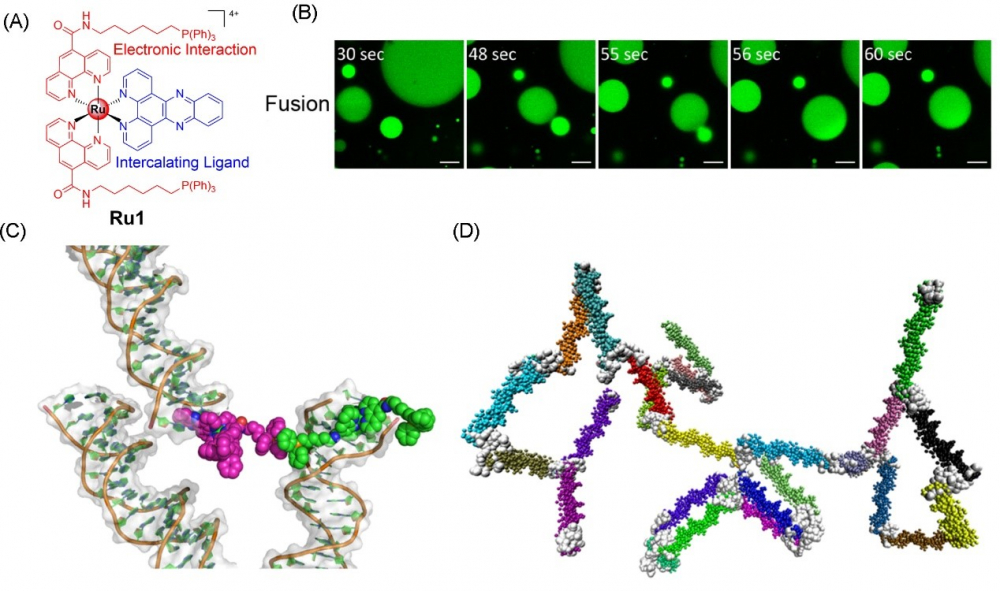
图1 (A)配合物Ru1的化学结构;(B)Ru1诱导DNA液-液相分离液滴的融合过程;(C)分子动力学模拟中Ru1与四分子DNA的结合模型;(D)分子动力学模拟粗粒化模型中Ru1与DNA的结合过程(2 μs)。
Ru1可以依次定位于线粒体和细胞核,并在活细胞中诱导DNA LLPS发生。通过使用Airyscan超高分辨成像技术和双光子磷光寿命成像技术,Ru1可以实时示踪活细胞内DNA LLPS的过程(图2)。转座酶可及染色质测序(ATAC-seq)测序和RNA测序表明Ru1可以改变染色质状态和基因表达谱。此外,Ru1可诱导线粒体自噬和细胞凋亡,并在体外筛选和荷瘤裸小鼠体内实验中显示出强大的抗癌活性。综上所述,该研究对小分子作为DNA LLPS诱导剂的分子结构设计提供了新思路,阐明了其对染色质状态和基因表达的影响,并证明调控DNA LLPS过程可能是一种有效的抗癌新策略。

图2(A)Airyscan超分辨成像和(B)双光子磷光寿命成像对Ru1诱导活细胞诱导DNA相分离过程进行示踪。
这一成果近期发表在Journal of American Chemical Society 上,文章的第一作者是永利集团3044noc登录入口2018级博士研究生汪文锦和中科院大连化学与物理研究所的助理研究员穆霞。
相关链接:https://pubs.acs.org/doi/10.1021/jacs.1c01424

